|
— Ь |
![]()
|
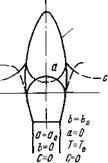
Рис. 9-3. Структура ламинарного диффузионного факела. а, Ь и с — концентрация газа, кислорода и продуктов сгорания. |
![]()
|
А=0-, Ъ-0 С=макс-, Тмакс фронт пламени |
 В случае, когда через горелку подается газ, не содержащий в себе кислорода, при его поджигании горение происходит за счет потребления кислорода окружающего воздуха, поступающего посредством диффузии. Так как в данном случае газ и воздух подаются раздельно, а горение происходит в — процессе их взаимной диффузии, причем скорость горения определяется интенсивностью процесса смешения, то подобное горение называют диффузионным.
В случае, когда через горелку подается газ, не содержащий в себе кислорода, при его поджигании горение происходит за счет потребления кислорода окружающего воздуха, поступающего посредством диффузии. Так как в данном случае газ и воздух подаются раздельно, а горение происходит в — процессе их взаимной диффузии, причем скорость горения определяется интенсивностью процесса смешения, то подобное горение называют диффузионным.
В зависимости от характера движения различают ламинарное диффузионное горение и турбулентное диффузионное горение.
Ламинарное диффузионное горение происходит при ламинарном режиме движения газа, вытекающего из горелки. Кислород, необходимый для горения, поступает из окружающей атмосферы и смешивается с горючим газом; получаемая в результате молекулярной диффузии смесь при поджигании образует факел, который при круглых горелках принимает конусообразную форму, так как по мере движения газ расходуется на горение и зона горения перемещается к оси струи, доходя до нее в вершине конуса (рис. 9-3).
Ламинарный диффузионный факел поддерживается стационарно, так же как при горении однородной смеси, за счет существования кольцевой зоны зажигания. В случае, когда в горелку подается только газ, а окружающая среда находится в покое, у кромки горелки газ диффундирует наружу и, смешиваясь с воздухом, образует смесь, которая в зоне малых скоростей устойчиво сгорает. Благодаря образованию более богатой смеси в области зажигающего кольца и сгоранию ее в зоне меньших скоростей диффузионный факел обладает большей устойчивостью зажигания по сравнению с факелом однородной смеси.
При диффузионном горении также наблюдается явление отрыва факела. Но проскок пламени в горелку исключается из-за раздельной подачи горючего газа и воздуха.
Зона устойчивого горения устанавливается по поверхности, где поступающие молекулярной диффузией количества газа и кислорода находятся в стехиометрическом соотношении для полного горения. Это утверждение следует из того, что в зоне горения не может быть ни избытка газа, ни избытка кислорода, так как в противном случае она не может занять устойчивого положения.
Предположим, что процесс горения установился в зоне, где имеется избыток горючего. В этом случае несгоревшая часть газа будет диффундировать в пространство вне факела, где, встретившись с кислородом, воспламенится за счет тепла, распространяющегося от фронта пламени, и сгорит, связав часть кислорода, поступающего в предполагаемую зону горения. Следовательно, количество кислорода, поступающего в нее, уменьшится, что еще более увеличит избыток газа. Поэтому предполагаемая зона горения не может занять устойчивого положения.
Предположим теперь, что процесс горения установился в зоне, где имеется избыток кислорода. Избыток кислорода, который не мог участвовать в реакции, должен диффундировать внутрь факела, где израсхо
дуется на окисление некоторой части газа, поступающего в предполагаемую зону горения. Такое течение процесса приведет к уменьшению количества газа, поступающего в зону горения, поэтому зона горения не может занять устойчивого положения. Отсюда единственно реальным является предположение о том, что диффузионное горение идет устойчиво по поверхности, где образующаяся смесь газа и кислорода соответствует стехиометрическому составу.
Таким образом, можно представить, что ламинарное диффузионное горение совершается следующим образом. Газ, вытекая из горелки, молекулярной диффузией смешивается с кислородом воздуха, полученная горючая смесь при поджигании образует достаточно резко очерченный конусообразный светящийся факел. Фронт пламени устанавливается по поверхности, где смесь образуется в пропорции, теоретически необходимой для горения. В зону горения изнутри поступает газовое топливо в виде различных основных и промежуточных продуктов, а снаружн — кислород. Образующаяся горючая смесь воспламеняется за счет тепла, распространяющегося от фронта пламени. Химическое превращение совершается в узкой светящейся зоне фронта горения в смеси, которая значительно разбавлена горячими продуктами сгорания и тем самым сильно нагрета, но в которой концентрации горючих элементов и окислителя малы. В таких условиях химическое реагирование протекает наиболее интенсивно. Толщина зоны горения мала — не превышает 1 мм.. Образующиеся продукты сгорания диффундируют как в окружающее пространство, так и внутрь факела. Поверхность пламени отделяет окислительную область вне факела, в которой имеются кислород и продукты сгорания и нет горючего, от восстановительной области внутри факела, в которой нет кислорода, но есть газ и продукты сгорания.
Структура ламинарного диффузионного факела показана на рис. 9-3. Концентрация горючего газа а падает от наибольшего значения на оси струи до нуля во фронте пламени, а концентрация кислорода Ь возрастает от нуля во фронте пламени до его значения в окружающем потоке. Концентрация продуктов сгорания с максимальна во фронте. Спектрографические исследования показали, что в пламени углеводородных топлив также находятся промежуточные вещества ОН, СН, С2.
Скорость химических реакций во фронте пламени обычно велика и несоизмерима больше, чем скорость поступления к нему компонентов горючей смеси. Поэтому скорость горения всецело определяется скоростью смешения газа и кислорода за счет их диффузии в зоне горения через слой продуктов сгорания.
Благодаря большой скорости химической реакции поступающие в зону горения газ и кислород практически мгновенно сгорают, в результате чего в зоне горения их концентрации практически равны нулю, а температура равна адиабатической. Большая скорость химической реакции обусловливает малую толщину пламени и позволяет рассматривать ее как геометрическую поверхность, с одной стороны которой находится смесь воздуха с продуктами сгорания, а с другой — смесь газа с продуктами сгорания.
Исходя из того, что скорость диффузионного горения не зависит от химической кинетики и определяется условиями смешения, можно аналитически рассчитать размер и форму фронта пламени как геометрическую поверхность, где скорость диффузии газа наружу и скорость диффузии кислорода внутрь таковы, что здесь количества газа и кислорода находятся в стехиометрическом соотношении для полного сгорания.
Так как скорость ламинарного диффузионного горения определяется скоростью молекулярной диффузии в ламинарно-движущемся потоке,, этот вид горения не может быть интенсивным, а возможен при малых скоростях выхода горючего газа из горелки.
Для определения длины ламинарного диффузионного факела воспользуемся известным выражением для времени диффузии воздуха до> оси горелки:
(9-16)
В формуле:
Я — радиус горелки;
И — коэффициент молекулярной диффузии.
Длина ламинарного диффузионного факела определяется как расстояние, проходимое газом за это время, т. е.
Г = 1Гт = -|^. (9-17)
Следовательно, длина ламинарного диффузионного факела прямо пропорциональна скорости истечения, квадрату радиуса горелки (или квадрату ширины щели для щелевых горелок) и обратно пропорциональна коэффициенту диффузии.
С увеличением теплоты сгорания газа в результате увеличения количества необходимого для горения воздуха длина факела увеличивается.
Объем газа, подаваемого за единицу времени в круглых горелках,
Q~WR^ (9-18)
А в щелевых
<3~УРЬ, (9-19)
Где Ь — ширина выходной щели горелки.
Поэтому при постоянном объемном количестве подаваемого газа длина факела круглой горелки согласно (9-17)
0_
Я ’
|
/ |
![]() (9-20}
(9-20}
А щелевой
(9-21)
Из (9-20) и (9-21) следует, что при постоянном объемном расходе газа длина факела при круглых горелках не зависит от их диаметра и скорости истечения, при щелевых горелках длина факела пропорциональна их ширине.
|
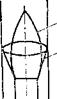
Рис. 9-4. Схема ламинарного пламен» в концентрических потоках. |

|
* I I Газ Воздух Воздух |
![]() Диффузионное пламя образуется также на поверхности соприкосновения газа и окислителя, двигающихся параллельно друг другу в свободном пространстве или канале. В последнем случае форма факела зависит от отношения количества подаваемого воздуха к теоретически необходимому его количеству^ При а>1 образуется стационарное замкнутое пламя в виде конуса с вершиной на оси канала (рис. 9-4, поверхность 1), а при а<1 —раскрытое пламя в виде чашки (рис. 9-4, поверхность 2).
Диффузионное пламя образуется также на поверхности соприкосновения газа и окислителя, двигающихся параллельно друг другу в свободном пространстве или канале. В последнем случае форма факела зависит от отношения количества подаваемого воздуха к теоретически необходимому его количеству^ При а>1 образуется стационарное замкнутое пламя в виде конуса с вершиной на оси канала (рис. 9-4, поверхность 1), а при а<1 —раскрытое пламя в виде чашки (рис. 9-4, поверхность 2).
В заключение следует отметить особенность диффузионного вида горения, связанную с наличием химической неполноты горения. В диф —
•фузионном ламинарном пламени температура достигает максимального значения в зоне горения. Вытекающий из горелки газ до поступления в зону горения нагревается за счет тепла, распространяющегося от пламени как теплопроводностью, так и посредством диффузии горячих продуктов сгорания. Некоторые газы, как, например, водород и окись углерода являются теплостойкими и при нагреве до температур 2500— 3000 К сохраняют свою молекулярную структуру. Горение теплостойких газов происходит в прозрачном факеле бледно-голубого цвета.
Газы, содержащие углеводородные соединения, являются теплонестойкими. В случае сжигания этих газов нагрев в восстановительной зоне в отсутствие кислорода вызывает их разложение с образованием сажи и водорода. Разложение углеводородосодержащих газов протекает тем интенсивнее, чем выше температура, при этом одновременно возрастает доля образующихся тяжелых, сложных, трудно сжигаемых углеводородов. Например, разложение метана начинается при температуре около 680—700°С. При нагреве без доступа воздуха до 950°С разлагается 26% метана, а при нагреве до 1150°С — 90%.
Находящиеся в пламени мелкодисперсные частицы сажи и свободного углерода, размеры которых чрезвычайно малы и составляют десятые доли микрона, раскалившись за счет выделившегося при горении тепла, излучают более или менее яркий свет, вызывая свечение пламени. Эти твердые частицы реагируют в гетерогенном процессе с кислородом, поступающим за счет молекулярной диффузии.
Диффузионное горение частиц протекает сравнительно медленно, в результате чего часть свободного углерода и тяжелых углеводородов не успевает сгорать и в виде сажи покидает факел. Наличие углерода согласно равновесию С + С02=2С0 вызывает образование СО. Количество углерода, тяжелых углеводородов и СО, присутствующих в продуктах сгорания, определяет величину химического недожога.



 14 апреля, 2013
14 апреля, 2013  doctype
doctype  Опубликовано в рубрике
Опубликовано в рубрике