Топливо состоит из горючей массы и балласта. В состав горючей массы входят от двух до пяти элементов. Углеводородное топливо — естественный газ и легкое жидкое топливо — состоит только из двух элементов — углерода и водорода, причем содержание углерода от 3 до 6 раз превышает содержание водорода.
В тяжелом жидком топливе — мазуте, помимо углеводородов, содержатся смолы, асфальтены и другие органические соединения, в состав которых, кроме углерода и водорода, входят также сера, кислород и азот. Однако суммарное количество этих трех элементов во много раз меньше, чем углерода или водорода.
В горючей же массе некоторых видов твердого топлива содержание кислорода в несколько раз превышает содержание водорода, например в дровах оно больше в 7 раз.
В доменных, ваграночных и некоторых генераторных газах основным горючим компонентом является окись углерода, в которой содержание кислорода по массе больше, чем углерода.
Состав горючей массы топлива и содержание в нем балласта обусловливают теплотехнические и технологические Характеристики топлива.
Углерод. Важнейшим компонентом горючей Массы топлива является углерод. Его содержание в горючей массе различных видов топлива колеблется от 50 до 99%. Округленное содержание углерода в горючей массе топлива приведено в табл. 13.
Таблица 13
|
Содержание углерода в горючей массе топлива
|
Содержащийся в топливе углерод входит в состав сложных органических соединений, образующих горючую массу топлива.
При сгорании 1 кг-атома углерода в виде графита выделяется около 94 000 ккал тепла, или около 7830 ккал’на 1 кг углерода.
Количество тeплaJ выделяющееся при сгорании углерода, содержащегося в различных видах топлива, неодинаково вследствие разной затраты энергии на разрыв связей между атомами в молекулах неоднотипных органических соединений.
Д. И. Менделеев установил, что различие в количестве тепла, выделяемого при сгорании углерода, входящего в состав разных видов твердого и жидкого топлива, сравнительно невелико и количество тепла, выделяемого при сгорании 1 кг углерода, может быть принято в среднем равным 8100 ккал.
В теплотехнических расчетах обычно принимают, что при сгорании 1 кг-атома углерода, содержащегося в трердом и жидком топливе, выделяется 97 650 ккал тепла.
Жаропроизводительность графита, т. е. максимальная температура, развиваемая при отсутствии потерь тепла, равна 2175 °С. Если принять теплому сгорания углерода, входящего в состав различных видов твердого и жидкого топлива, по Д. И. Менделееву, равной 8100 ккал/кг, то жаропроизводительность углерода топлива составит 2240 °С.
Водород. Вторым по значению компонентом топлива является водород. Вг0. содержание в горючей массе различных видов топлива (округленно) дано в табл. 14.
|
Таблица 14 Содержание водорода в горючей массе топлива
|
При сгорании 1 кмоль газообразного водорода, с образованием воды, выделяется 68 260 ккал тепла, т. е. 33 860 ккал на 1 кг газообразного водорода, при 3046 ккал на 1 м3 водорода при нормальных условиях (температура 0°С, давление 1 кгс/см2).
Следовательно, при сгорании 1 кг газообразного водорода выделяется в 4,2 раза больше тепла, чем при сгорании 1 кг углерода. Поэтому теплота сгорания топлива значительно возрастает с повышением содержания в нем водорода. Так, теплота сгорания горючей массы кокса с минимальным содержанием водорода равна около 8000 ккал/кг, а теплота сгорания мазута, состоящего примерно из 88% углерода и 12% водорода, — более 10 000 ккал/кг. Теплота сгорания 1 кг метана, состоящего из 75% углерода и 25% водорода, еще выше и равна ~ 12 000 ккал.
Продукты сгорания отводят из котлов и печей обычно при температуре, превышающей 100 °С. В этих условиях в дымовых газах содержится не вода, а водяной пар. На нагревание и испарение 1 кг влаги расходуется около 600 ккал.
С учетом расхода тепла на испарение воды при сгорании килограмм — молекулы водорода выделяется 57 740 ккал тепла, т. е. 28 640 ккал на 1 кг водорода, или 2576 ккал на 1 м3 Н2 при нормальных условиях.
Количество тепла, выделяющееся при сгорании 1 кг водорода с образованием воды, называется высшей теплотой сгорания, а количество тепла, выделяющееся при сгорании 1 кг водорода с образованием водяного пара, — низшей теплотой сгорания.
Отношение высшей теплоты сгорания водорода к низшей составляет 68260: 57 740, т. е. около 1,18. В соответствии с этим у топлива, в состав которого входит значительный процент водорода, высшая и низшая теплота сгорания существенно различаются.
При сжигании природного газа и других видов бессернистого топлива с высоким содержанием водорода есть возможность охладить продукты сгорания ниже точки росы и использовать теплоту конденсации содержащегося в них водяного пара.
В этих условиях возможное использование потенциального тепла топлива определяется его высшей теплотой сгорания и количество использованного тепла может превосходить низшую теплоту сгорания топлива.
При сгорании водорода, содержащегося в твердом и жидком топливе, выделяется несколько меньше тепла, чем при сгорании молекулярного газообразного водорода.
Содержащийся в топливе водород подобно углероду входит в состав различных органических соединений, теплота разложения которых неодинакова. Поэтому при сгорании 1 кг водорода, содержащегося в различных видах твердого и жидкого топлива, выделяется различное количество тепла. Это различие, впрочем, не очень велико. Д. И. Менделеев установил, что 1 кг водорода, содержащийся в различных видах твердого и жидкого топлива, выделяет при сгорании в воду около 30 000 ккал тепла, а при сгорании в водяной пар — 24 600 ккал (на 4000 ккал меньше, чем 1 кг молекулярного газообразного водорода).
Жаропроизводительность молекулярного водорода равна 2235 °С, т. е. близка к жаропроизводительности углерода, несмотря на большое различие в теплоте сгорания углерода и водорода.
Закономерность этого весьма важного положения обоснована при обсуждении жаропроизводительности топлива.
Содержание водорода в горючей массе повышает реакционную способность и скорость горения топлива.
Повышение содержания водорода в горючей массе твердого топлива обусловливает увеличение выхода летучих веществ, выделяющихся при нагревании топлива без доступа воздуха.
Содержание углерода и водорода в топливе определяют, сжигая небольшую навеску (0,3—0,5 г) сухого топлива в токе кислорода. Газообразные продукты сгорания пропускают через контактную массу, состоящую из раскаленной окиси меди, что обеспечивает полноту окисления продуктов неполного сгорания до углекислого газа и водяного пара’
СО + СиО = Си + С02, Н2 + СиО = Си + Н20.
Затем образующийся водяной пар поглощают серной кислотой или прокаленным хлористым кальцием, а углекислый газ — едким кали.
По увеличению веса поглотителей определяют количество водяного пара и углекислого газа и в соответствии с этим подсчитывают содержание углерода и водорода в навеске исследуемого топлива.
При определении содержания углерода и водорода применяемый кислород очищают от следов углекислого газа и водяного пара при помощи поглотителей — натронной извести Ca(OH)2NaOH, хлористого кальция CaCU и концентрированной серной кислоты, а продукты сгорания перед пропусканием их через окись меди освобождают от сернистого газа (образующегося в результате сгорания содержащейся в топливе серы), который поглощается хромокислым свинцом с образованием сернокислого свинца.
Процесс сгорания топлива и полного окисления образующихся газообразных продуктов реакции путем контакта с окисью меди ведут при температуре ~800 °С, а очистку продуктов сгорания от сернистого газа—при 600 °С.
Топливо и поглотительные сосуды взвешивают на аналитических весах с точностью до 0,0002 г.
Содержание углерода в топливе определяют по формуле
С=.(Л14^0,273.100 %> (П1)
Где Аі — привес кали-аппарата с раствором едкого кали, г; Az — привес контрольной ^/-образной трубки с натронной известью; г; 0,278— = 12 : 44 — коэффициент для пересчета С02 ‘в С; В — наївеска исследуемого топлива, г.
Кислород. Третий важный компонент горючей массы топлива — кислород. Содержание его в горючей массе различных видов топлива (округленно) приведено в табл. 15.
Таблица 15
|
Содержание кислорода в горючей массе топлива
|
Высоким содержанием кислорода характеризуется горючая масса растительного топлива, а также молодых видов ископаемого топлива — торфа и бурых углей. Значительно меньше кислорода содержится в каменных углях. В антраците содержание кислорода составляет 1—2%.
Малое содержание кислорода характерно также для искусственных видов обуглероженного твердого топлива, получаемых из угля, торфа или древесины отгонкой из них летучих веществ.
Содержащийся в горючей массе кислород снижает ее теплоту сгорания. Это обусловлено двумя факторами. Во-первых, кислород в горючей массе топлива соответственно уменьшает процентное содержание в ней углерода и водорода, обладающих высокой теплотой сгорания. Кислород же является как бы балластом, входящим непосредственно в состав органических соединений, образующих горючую массу топлива. Во-вторых, кислород, входящий в состав горючей массы, находится в химическом соединении с водородом и углеродом, например в виде гидроксильных (ОН) и карбоксильных (СООН) групп, т. е. водород и углерод присутствуют частично в окисленном состоянии, что существенно снижает количество тепла, выделяемого при их сгорании (доокислении).
Степень снижения теплоты сгорания горючей массы топлива вследствие содержания в ней кислорода зависит от состава кислородсодержащих соединений и от того, с каким элементом — водородом или углеродом— химически связан кислород.
При взаимодействии углерода с кислородом с образованием углекислого газа по уравнению С+02=С02 выделяется 97 650 ккал на 1 кмоль вступающего в реакцию кислорода.
При взаимодействии водорода, содержащегося в твердом или жидком топливе, с кислородом с образованием водяного пара по формуле Н24-0,502=Н20 выделяется 98400 ккал на 1 кмоль кислорода. Таким образом, при соединении кислорода с водородом выделяется тепла лишь на 1%-больше, чем при соединении такого же количества кислорода с углеродом.
Д. И. Менделеев установил, что содержание 1% кислорода в горючей массе топлива снижает ее теплоту сгорания вследствие частичного окисления углерода и водорода в среднем на 26 ккал/кг.
При сопоставлении двух указанных выше причин снижения теплоты сгорания горючей массы топлива вследствие содержания в ней кислорода становится очевидным, что первая причина (снижение содержания углерода и водорода) имеет большее значение, чем вторая. В самом деле, уменьшение содержания водорода в горючей массе на 1% снижает низшую теплоту ее сгорания на 246 ккал/кг, уменьшение содержания углерода на 1% —соответственно на 81 іккал/кг, а дополнительное — снижение теплоты сгорания вследствие частичного окисления углерода и водорода горючей массы составляет 26 ккал/кг.
Теплота сгорания 1 кг горючей массы древесины из-за высокого содержания кислорода (около 44%) ‘Примерно в 2 раза ниже теплоты сгорания горючей массы антрацита или кокса и в 2,5—3 раза ниже теплоты сгорания углеводородного топлива. Топливо с высоким содержанием кислорода в горючей массе — древесина, торф, молодые бурые угли — обладает высокой гигроскопичностью и содержит много влаги. У этих видов топлива теплота сгорания влажной рабочей массы значительно ниже теплоты сгорания горючей массы.
Кислород в горючей массе твердого топлива сравнительно мало снижает ее жаропроизводительность, однако высокая влажность топлива с большим содержанием кислорода обусловливает увеличение объема продуктов сгорания вследствие испарения влаги и снижение в результате этого температуры, развиваемой при сжигании топлива.
Твердое топливо с большим содержанием кислорода в горючей массе характеризуется высоким выходом летучих веществ, легко зажигается и обладает высокой реакционной способностью. В легком дистиллированном жидком топливе практически нет кислорода. В сырой нефти и мазуте, хотя и в незначительном количестве, содержится кислород, входящий в состав смол и нафтеновых кислот. В природных и нефтезаводских газах кислорода весьма мало (входит в состав окислов углерода). В коксовых, генераторных и доменных газах присутствует значительное количество связанного кислорода (в виде СО и СОг), а содержание свободного молекулярного кислорода обычно не превышает 1%.
Содержание кислорода в газе (в процентах по объему) определяют путем его поглощения пирогаллолом, а в горючей массе твердого топлива (в процентах по массе) фиксируют по разности после определения остальных компонентов горючей массы топлива:
Ог=ЮО % — (Cr + Hr + S;+K + Nr) %.
Азот. Содержание азота в горючей массе твердого топлива колеблется от 0,6 (дрова) до 2% У некоторых видов углей и торфа.
При коксовании каменных углей в атмосфере, не имеющей свободного кислорода, азот, содержащийся в топливе, в значительной степени выделяется в виде аммиака NH3.
В нефти содержание азота обычно колеблется от 0,03 до 0,3%.
В газообразном топливе основным видом балласта является азот — от долей процента в некоторых природных и нефтепромысловых газах до 60% в доменных и 75% в ваграночных газах. Газы с высоким содержанием азота характеризуются низкой теплотой сгорания и пониженной жаропроизводительностью.
Содержание азота в твердом и жидком топливе определяют по методу Кьелдаля, основанному на способности кипящей серной кислоты окислять органические соединения до С02 и Н20, а содержащийся в, них азот превращать в NH3. Образующийся аммиак улавливают серной кислотой и по количеству NH3 определяют содержание азота в топливе.
В газообразном топливе азот фиксируют как остаточный член после определения содержания в газе других компонентов:
N2=100% — (С02 + 02 + С0 + Н2 + СН4 + и т. д.) %.
В процессе горения азот топлива переходит в дымовые газы в виде молекулярного азота N2, а при высокой температуре в топках и печах частично окисляется с образованием весьма вредных для здоровья окислов азота.
Азот, входящий в состав сложных органических соединений, окисляется при значительно более низкой температуре, чем молекулярный азот, входящий в состав воздуха и газообразного топлива. Поэтому загрязнение воздушного бассейна окислами азота, содержащимися в продуктах сгорания, в значительной степени зависит от содержания в топливе связанного азота.
До сравнительно недавнего времени азот в топливе рассматривали лишь как балласт, несколько снижающий его теплоту сгорания. Однако по мере выяснения роли азота топлива в образовании токсичных окислов азота содержание связанного азота, входящего в состав твердого и жидкого топлива, рассматривается как весьма нежелательное.
Азот, содержащийся в нефти, входит в основном в состав нефтяных смол и асфальтенов. Поэтому в процессе очистки нефти от смол и ас — фальтенов содержание азота соответственно снижается.
В легком дистиллированном жидком топливе — бензине и керосине — практически не содержится азот, а в нефтяных остатках, получаемых в процессе перегонки нефти, — мазуте азот содержится в большем количестве, чем в сырой нефти.
Сера. В топливе содержатся три вида серы: органическая, колчеданная (пиритная) и сульфатная.
Органическая сера S0 входит в состав сложных органических соединений, образующих топливо. При сжигании топлива органическая сера сгорает с образованием сернистого газа с выделением 69 800 ккал на 1 кг-атом серы (S + 02=S02+69800 ккал), или около 2 180 ккал на 1 кг серы.
Колчеданная, или пиритная, сера SK содержится в твердом топливе. Она входит в состав железного колчедана FeS2 и других сернистых соединений. При сжигании твердого топлива колчедан сгорает с образованием сернистого газа и окислов железа.
4FeS2 +1102=2Fe203 + 8S02
С выделением около 200000 ккал тепла на 1 моль колчедана; при этом вследствие сгорания серы выделяется около 140 000 ккал, а в результате окисления железа — около 60 000 ккал. При пересчете всего количества тепла, выделяющегося при сгорании колчедана, т. е.
200000 ккал/моль, на содержащуюся в нем серу получают «кажущийся» тепловой эффект, равный примерно 3100 ккал на 1 кг серы.
При подсчетах теплоты сгорания твердого и жидкого топлива можно принять, что на 1 кг горючей серы выделяется в среднем около 2600 ккал, или 26 ккал на 1% горючей серы, содержащейся в 1 кг топлива. Таким образом, содержание серы несколько снижает теплоту сгорания топлива, особенно высококалорийного.
Таблица 1&
|
Содержание серы в горючей массе топлива и приведенная сернистость рабочего топлива
|
Данные о содержании горючей серы (органической и колчеданной) в различных видах топлива приведены в табл. 16. Там же дано процентное содержание горючей серы в топливе, пересчитанное на 1000 ккал низшей теплоты сгорания (<2Й), т. е. показана приведенная сернистость топлива:
Snp„B = 1000Sr:QE.
Сера резко понижает народнохозяйственную ценность топлива, особенно технологического. Содержащаяся в коксе сера частично переходит в выплавляемый металл, который становится ломким при высокой температуре. Во избежание этого серу кокса химически связывают известью и переводят в шлаки. Увеличение содержания серы в коксе на 1% обусловливает повышение расхода флюсов и топлива примерно на 15%. При этом значительно снижается производительность доменных печей.
Помимо органической и колчеданной серы, в топливе содержится небольшое количество полностью окисленной сульфатной серы, входящей в состав CaS04, FeSOi и других сернокислых солей. При сжигании топлива сульфатная сера переходит в золу и вследствие этого мало влияет на свойства топлива.
В жидком топливе сера содержится преимущественно в виде органических соединений. Производство моторного топлива и смазочных масел из высокосернистой нефти крайне осложняется необходимостью их очистки от сернистых соединений.
В газообразное топливо сера входит в виде сероводорода H2S и частично сероуглерода CS2 и других органических соединений.
При высоком содержании горючей серы в котельном топливе дымовые газы сильно загрязнены сернистым ангидридом SO2, губительно действующим на металлические поверхности и растительность. При сжигании сернистого топлива с избытком воздуха S02 частично окисляется до S03 с образованием серной кислоты (S03+H20=H2S04),
|
|
|
Рнс. 3. Точка росы продуктов сгорания сернистого топлива / — а=1,15, 2 — а=1,10, 3 — а=1,05 |
Оказывающей сильное корродирующее действие на металл, особенно при температуре, близкой к точке росы паров серной кислоты. Температура конденсации водяных паров, содержащихся в продуктах сгорания топлива, зависит от парциального давления НгО. При парциальном давлении Н20 порядка 0,1 ат (например, при сжигании мазута с небольшим избытком воздуха) точка росы равна около 45 °С.
Однако при сжигании сернистого топлива приходится считаться с точкой росы, обусловленной конденсацией не водяного пара, а паров серной кислоты. На рис. 3 показана точка росы продуктов сгорания сернистого топлива в зависимости от содержания в них S03.
При температуре, близкой к точке росы, наблюдается сильная коррозия поверхностей нагрева котлов. Во избежание этого дымовые газы отводят из котлоагрегатов при более высокой температуре, что снижает КПД котельной установки.
Для предотвращения коррозии стремятся сжигать сернистое топливо с минимальным избытком воздуха (примерно 2—3%) и тем самым не допустить окисления SO2 в SO3.
Чтобы уменьшить загрязнение воздушного бассейна городов окислами серы, создают установки для очистки дымовых газов и сооружают дорогостоящие высокие дымовые трубы.
Определение содержания серы в топливе. Определение в твердом топливе содержания общей серы состоит из следующих операций:
1. Сжигание навески топлива.
2. Поглощение образующихся при сжигании окислов серы смесью Эшка, состоящей из 67% MgO и 33% Na2C03, с образованием сернокислых солей магния и натрия:
Mg0 + S03 = MgS04,
Na2COs + S03 = Na, S04 + С02.
3. Растворение образующихся сернокислых солей в горячей воде.
4. Осаждение сернокислых соединений в виде нерастворимого в воде сернокислого бария
MgS04 + ВаС12 = BaS04 + MgCl2.
5. Отделение осадка сернокислого бария на фильтре, высушивание, сжигание фильтра и прокаливание осадка сернокислого бария.
23
6. Взвешивание сернокислого бария и подсчет содержащейся в нем серы.
Содержание серы подсчитывают по формуле
Где S — содержание серы в топливе, %; В — вес прокаленного сернокислого бария, г; А — навеска угля, г; 0,1373=32/гзз — коэффициент, показывающий содержание серы в сернокислом барии (S/BaS04).
При содержании до 2% S расхождения в определении в одной лаборатории не должны превышать 0,05% и в разных лабораториях 0,1%, а при большом содержании серы — соответственно 0,1 и 0,2%.



 2 сентября, 2012
2 сентября, 2012  admin
admin 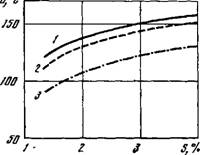
 Опубликовано в рубрике
Опубликовано в рубрике