Зажигание, как и самовоспламенение, характеризует условия возникновения горения. Эти явления имеют одинаковую природу, описываются одними и теми же дифференциальными уравнениями.
В случае самовоспламенения подводимое к реагирующей системе тепло распределяется по всему объему этой системы. Реакция горения при самовоспламенении протекает практически одновременно во всем объеме системы, а начальный очаг горения возникает в ее центре, где потери тепла минимальны. Одним из наиболее важных параметров при самовоспламенении является объем реагирующей смеси, поскольку от этого параметра существенно зависит отвод тепла в окружающее пространство.
При зажигании* в отличие от самовоспламенения нагревается небольшой объем горючей смеси. Зажигание, т. е. инициирование горения может быть осуществлено накаленным телом, пламенем или электрической искрой. Механизм процесса зажигания близок к механизму самовоспламенения, но более сложен. Критические условия зажигания зависят от свойств горючей смеси, от свойств источника зажигания и от начальных условий распространения пламени.
Основной отличительной особенностью зажигания является протекание реакции окисления, инициируемое локальным источником тепла, а не путем накопления тепла в системе за счет реализации химической реакции. Для процесса зажигания определяющим является наличие большой разности температур между горючей системой и источником зажигания. Размеры системы играют второстепенную роль.
Для выяснения механизма зажигания рассмотрим схему, предложенную Вант-Гоффом (рис. 3.3). Зависимости, представленные на этом
* В теории горения процесс зажигания горючей смеси часто обозначается термиНами «вынужденное зажигание» и «вынужденное воспламенение».
53
Корольченко А. Я. Процессы горения и взрыва
Рисунке, характеризуют изменение температуры среды при попадании в нее накаленного шарика. Линии А1, а2 И А3 Отражают изменение температуры инертной среды, линии B1, B2И bЗ — горючей.
|
|
Рис. 5J. Изменение температуры смеси
В зависимости от температуры
Поверхности шарика
Вначале, температура Т1 Поверхности шарика, играющего роль источника зажигания, выше температуры газовой смеси, но ниже той температуры, при которой происходит воспламенение смеси. В этом случае распределение температуры T вблизи поверхности шарика изобразится кривой a1 (для инертной среды) и кривой b1- для горючей. Кривая b1 располагается несколько выше a1 за счет тепловыделения в горючей среде.
Если повысить температуру шарика Т2 > T1, то в инертной среде она будет понижаться быстрее, чем в предыдущем случае. Ее снижение характеризует кривая A2_. В реагирующей смеси, благодаря возрастанию скорости реакции с повышением темпе-
54
Глава 3. Возникновение процессов горения
Ратуры, кривая T(Z) Вблизи поверхности шарика будет снижаться медленнее, чем в предыдущем случае. Но величина этой температуры еще не достаточна для возбуждения реакции горения. Температура Т2 Является критической температурой, аналогичной температуре самовоспламенения. При повышении температуры поверхности шарика выше критической, например до температуры Т3, В горючей смеси инициируется горение. При этом поверхность уже не участвует в процессе, а определяющими становятся свойства горючей смеси.
Экспериментальные данные свидетельствуют о том, что критическая температура при зажигании выше, чем при самовоспламенении. Это связано с быстрым падением температуры газовой смеси по мере удаления от поверхности нагретого тела. При этом концентрация горючего компонента вблизи поверхности вследствие протекания химической реакции оказывается ниже, чем в остальном объеме. В экспериментах наблюдаются ситуации, когда около нагретого тела реакция протекает, но далее пламя не распространяется.
Математическое описание процесса зажигания выполнено академиком Я. Б. Зельдовичем. Для этого использована следующая модель: горючая газовая смесь заключена между двумя бесконечными плоскими параллельными стенками. Одна стенка имеет температуру Ts, А вторая — Т0 (при этом TS>T0) Стационарное распределение температуры в газовой смеси устанавливается только в том случае, когда температура нагретой стенки не превышает критическую величину и около нее не происходит химическая реакция. При критических условиях, по аналогии с процессом самовоспламенения
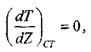 (3.12)
(3.12)
Где Z — расстояние от нагретой стенки; индекс «СТ» Указывает на то, что градиент температуры относится к слою газа у поверхности стенки.
Распределение температуры в газе описывается уравнением теплопроводности, которое для рассматриваемого случая имеет вид:
![]() (3.13)
(3.13)
Где ![]() — коэффициент теплопроводности газовой смеси, Q — Тепловой эффект,
— коэффициент теплопроводности газовой смеси, Q — Тепловой эффект, ![]() — скорость реакции.
— скорость реакции.
55
Корольченко А. Я. Процессы горения и взрыва
Скорость реакции зависит от температуры по закону Аррениуса:
|
|
(3-14)
![]() Введем новую переменную
Введем новую переменную
|
|
И уравнение (3.13) запишем так:
|
|
(3.15)
Интегрируя (3.15), получим:
|
|
(3.16)
Отсюда следует, что поток тепла в газовой смеси отвечает соотношению:
|
|
(3-17)
Поскольку скорость реакции зависит от температуры, то реакция в газовой смеси между стенками будет в основном протекать в узком слое ![]() , прилегающем к нагретой стенке. Внутри этого слоя величина Ts — Г при условиях, близких к критическим, будет мала по сравнению с Т.
, прилегающем к нагретой стенке. Внутри этого слоя величина Ts — Г при условиях, близких к критическим, будет мала по сравнению с Т.
Поэтому, можно принять:
|
|
|
|
И что
(3.18)
(3.19)
56
Глава 3. Возникновение процессов горения
Подставляя (3.19) в (3.15), интегрируя и принимая во внимание, что
(DT -п При критических условиях зажигания выполняется условие ~Rz ст — и s
Получим:
|
|
(3.20)
Эксперимент показывает, что величина
|
|
При изменении Ts— T На десятки градусов меняется в узких пределах: от 1 до 0,4. Следовательно, значение У Вне зоны ![]() Незначительно отличается от величины
Незначительно отличается от величины
|
|
Таким образом, тепловой поток из зоны реакции будет равен:
|
|
(3.21)
Величину этого теплового потока при установившемся состоянии можно представить в упрощенном виде:
|
|
(3.22)
Отсюда следует, что при стационарном режиме выполняется следующее равенство:
|
|
(3.23)
57
Корольченко А. Я. Процессы горения и взрыва
Соотношение (3.23) устанавливает зависимость критических величин и условий, при которых реализуется Зажигание, От Размеров Сосуда.
Зажигание искрой горючей смеси представляет собой более сложное явление, чем зажигание нагретым телом. В искре происходит интенсивное местное возбуждение молекул и их ионизация. Одновременно искра в зоне своего действия вызывает сильное повышение температуры газа. В упрощенном виде искру можно представить как накаленное газообразное тело.
При зажигании искрой для каждой горючей смеси существует некоторая минимальная мощность искры, при которой смесь воспламеняется. Эта мощность зависит от состава смеси, давления и температуры. Характер этой зависимости от состава смеси показан На рис. 3.4. Он одинаков для всех горючих газов и паров. Наименьшая величина энергии требуется для зажигания смесей стехиометрического состава. Эта величина называется минимальной энергией зажигания. Значения минимальной энергии зажигания для некоторых газов Приведены В Табл. 3.1.
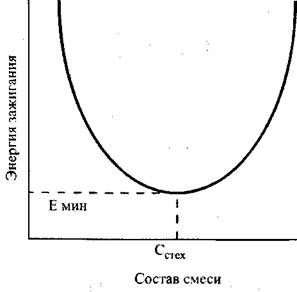
Рис. 3.4. Зависимость энергии зажигания от состава смеси Cстех — Стехиометрический состав; Емин — минимальная энергия зажигания
Глава 3. Возникновение процессов горения
Таблица 3.1 Минимальная энергия зажигания
|
Вещество |
Емин, МДж |
|
Метан |
0,28 |
|
Этан |
0,24 |
|
Пропан |
0,25 |
|
Бутан |
0,25 |
|
Гексан |
0,25 |
|
Аммиак |
680 |
|
Этилен |
0,12 |
|
Водород |
0,017 |



 4 мая, 2013
4 мая, 2013  admin
admin 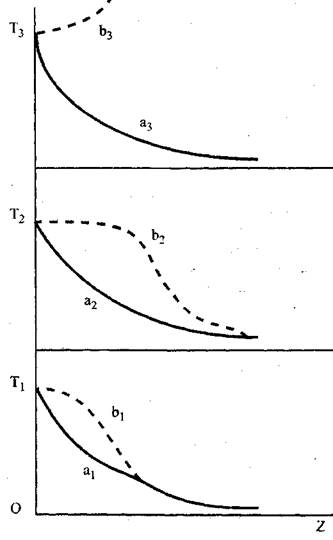
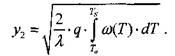
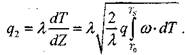
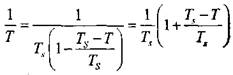
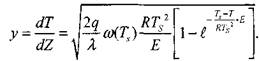
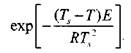
 Опубликовано в рубрике
Опубликовано в рубрике