Переход де-флаграционного горения в детонацию в газовоздушных смесях
Возможен в следующих случаях:
• при обогащении горючей смеси кислородом;
• при очень больших размерах газовых облаков;
• при наличии турбулизаторов горения.
Согласно теории гидродинамической неустойчивости и автотурбу-лизации фронта нормального горения в горючих облаках достаточно больших размеров неизбежен переход от дефлаграционного горения к детонации. Экстраполяционные оценки приводят к следующим критическим размерам облаков, при которых вероятность возникновения детонации высока: для водородовоздушных смесей — 70 м, для пропановоздуш-ных — 3500 м, для метановоздушных — 5000 м.
Турбулизация процесса горения газовых смесей с помощью различных препятствий по пути распространяющегося пламени приводит к существенному сокращению критических размеров газовых облаков, и возникающая в этом случае детонационная волна становится источником возбуждения детонации в неограниченном пространстве.
Проф. В. И. Макеевым экспериментально изучена возможность перехода дефлаграции в детонацию при горении смесей СН4 + 2(02 + ![]() N2) и
N2) и
2Н2 + 02 + ![]() N2 при значениях
N2 при значениях ![]() ‘ в интервале от 0 до 3,76 в объеме 6 м3 с
‘ в интервале от 0 до 3,76 в объеме 6 м3 с
91
Корольченко А. Я. Процессы горения и взрыва
Частично загроможденным пространством. Для загромождения использовались в различных комбинациях три тонкостенные металлические концентрически расположенные сферы-турбулизатора с большим количеством отверстий. Коэффициент проницаемости сфер составлял от 0,1 до 0,4, соотношение диаметров 1:2:4. Отношение объема, занятого турбулизатором к объему горючей смеси составляло от 0,01 до 0,48%. Горение инициировалось в центре сфер пережигаемой нихромовой проволочкой. Переход от дефлаграции к детонации наблюдался в смесяхСН4 +2(02 + ![]() N2) при
N2) при ![]() И в смесях 2Н2 + 02+N2
И в смесях 2Н2 + 02+N2 ![]() При
При ![]() < 3,2. С учетом полученных данных можно полагать, что для воздушных смесей (
< 3,2. С учетом полученных данных можно полагать, что для воздушных смесей ( ![]() = 3,76) водорода и метана критический размер загроможденного пространства, при котором возможен переход к детонации, составляет примерно 1 и 10 м соответственно.
= 3,76) водорода и метана критический размер загроможденного пространства, при котором возможен переход к детонации, составляет примерно 1 и 10 м соответственно.
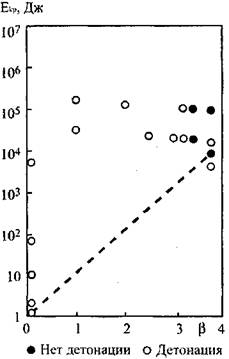
Зависимости критической энергии возбуждения детонации в загро
можденном пространстве для исследованных смесей от состава смеси по
казаны на Рис. 4.5 и 4.6. "
|
|
|
|
92
Рис. 4.5. Зависимость критической Рис. 4.6. Зависимость критической
Энергии возбуждения детонации Энергии возбуждения детонации
От состава смеси СН4+2(02+ ![]() N2) От состава смеси 2Н2+02+
N2) От состава смеси 2Н2+02+ ![]() N2
N2
Глава 4. Развитие горения
Расчет параметров детонационных волн в смесях водород-Кислород-инертный газ.* Детонационные волны, образующиеся прк сгорании газовых смесей, характеризуются следующими параметрами: скоростью детонации, температурой и давлением в детонационной волне.
Для определения этих параметров проф. Ю. Н. Шебеко с сотр. предложен метод расчета, основанный на рассмотрении химической реакции вида:
|
|
В диапазоне температур примерно до 5500 К другие компоненты в продуктах реакции не образуются в существенных количествах. Введем константу и, равную числу всех атомов, участвующих в химической реакции; в ходе реакции эта величина остается неизменной. Для П Имеем соотношение
|
|
|
|
Обозначим общее число молей вещества, участвующего в химиче-
|
Начальное число молей |
Ской реакции в точке равновесия, через
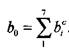
* При рассмотрении параметров детонационных волн приняты следующие обозначения:
|
|
Давление;
Плотность;
Температура;
— молярная масса г-ого компонента;
Скорость газа в системе скачка;
|
Молярные теплоемкости при постоянном давлении и ооъеме соответ- |
|
|
|
Ственно; |
|
Константы, определяемые исходным составом по формулам |
|
|
|
|
Полная удельная энтальпия;
|
|
Скорость звука в исходной смеси;
|
Расчетное значение давления в детонационной волне; рассчитанное значение температуры в детонационной волне; — экспериментально измеренное значение скорости детонации; — рассчитанное значение скорости детонации. |
|
|
Скорость детонации; скорость звука в продуктах реакции; температура в детонационной волне; давление в детонационной волне;
Корольченко А. Я. Процессы горения и взрыва
Введем мольную долю каждого компонента ![]() , и «мольные
, и «мольные
Доли» всех атомов ![]()
Полная система уравнений для расчета детонационных адиабат содержит четыре уравнения материального баланса по атомам (4.13)-(4.16); четыре уравнения химического равновесия (4.17)-(4.21); уравнение состояния (4.22); и три уравнения газодинамики: уравнение непрерывности (4.23); и два уравнения, являющиеся следствием закона сохранения плотности потока импульса (4.24) и энергии (4.25).
Уравнения материального баланса по атомам
(кислород) 2y1 +уз+ у4 + У5 = С1у0; (4.13)
(водород) 2у2 + уз + 2у4 + у6 = с2у0; (4.14)
(аргон) у7=с3у0;
у1+ у2 + уз + У4 + У5 + У6+С3У0= 1 (4.16)
Уравнения химического равновесия
|
Уравнение состояния: Уравнение неразрывности: |
|
|
|
(4.21) |
(4.17) (4.18) (4.19) 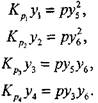 (4.20)
(4.20)
![]() (4.22) Уравнение сохранения потока импульса:
(4.22) Уравнение сохранения потока импульса:
![]() (4.23) Уравнение сохранения энергии:
(4.23) Уравнение сохранения энергии:
![]()
94
Глава 4. Развитие горения
Таким образом, система содержит 12 уравнений при 13 неизвестных (у0-у7) Р, р, Т, ![]() И. Чтобы замкнуть систему, необходимо дополнительное уравнение, называемое условием Чемпена-Жуге: равенство скорости газа И В системе волны и местной скорости звука
И. Чтобы замкнуть систему, необходимо дополнительное уравнение, называемое условием Чемпена-Жуге: равенство скорости газа И В системе волны и местной скорости звука ![]()
(4.25)
Где уf определяется равенством 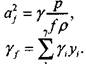
Система уравнений (4.13-4.24) позволяет сократить число переменных, выразив У1-Y4 Через У0 И У3-у7, А остальные переменные представив в безразмерном виде.
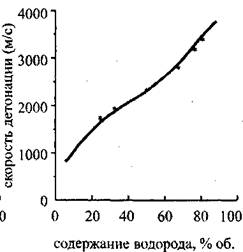
Состояния Чепмена-Жуге рассматриваются для начальной температуры 298,15 К при начальных давлениях до 0,25 МПа. В табл. 4.1. представлены результаты расчетов: параметры состояния Чепмена-Жуге для двенадцати составов исходной смеси, при стандартных начальных условиях (начальное давление равно 1 атм, температура 298,15 К). В табл. 4.2. представлены рассчитанные значения температуры, давления и скорости детонации для некоторых смесей. В третьей колонке этой таблицы даны экспериментально измеренные значения скорости детонации. Рис. 4.7 Иллюстрирует хорошее согласие расчетных значений с экспериментом для водородокислородной смеси в широком диапазоне концентраций водорода, а Рис. 4.8 — для гремучей смеси, разбавленной аргоном. Существенное возрастание скорости детонации, при превышении процентного содержания водорода в смеси стехиометрической отметки (67 %) объясняется уменьшением средней молярной массы смеси. Скорость фронта детонации зависит от удельного энерговыделения по закону ![]() Где Q Удельная эн-
Где Q Удельная эн-
Тальпия сгорания смеси, и, кроме того, от скорости звука в исходной смеси. Поэтому, даже когда молярное энерговыделение падает, скорость детонации растет за счет уменьшения молярной массы и увеличения скорости звука. Согласие экспериментальных и расчетных значений для смесей, содержащих инертный разбавитель (аргон), несколько хуже. График зависимости скорости детонации от содержания аргона в смеси, состоящей из двух молей водорода и одного моля кислорода представлен на Рис. 4.9. Там же отмечены точки, соответствующие экспериментально измеренной скорости детонации.
95
Корольченко А. Я. Процессы горения и взрыва______________________
Таблица 4.1. Результаты расчета для различных смесей водород-кислород-инертный разбавитель
|
Смеси |
А0, м/с |
U0 м/с |
А, м/с |
Т, °К |
Р, атм |
|
Но+407 |
365 |
1456 |
858 |
1977 |
10,17 |
|
Н2+302 |
376 |
1641 |
953 |
2398 |
12,18 |
|
Н2+1,502 |
416 |
2061 |
1179 |
3171 |
15 72 |
|
Н2+02 |
451 |
2331 |
1332 |
3458 |
16,98 |
|
1,5Н2+02 |
498 |
2631 |
1504 |
3631 |
17,76 |
|
2Н2+02 |
537 |
2867 |
1640 |
3684 |
18,14 |
|
Зн2+о2 |
604 |
3214 |
1838 |
3618 |
17,99 |
|
4Н2+02 |
658 |
3445 |
1967 |
3455 |
17,44 |
|
2Н2+О2+0,1 Аr |
520 |
2763 |
1587 |
3661 |
17,91 |
|
2Н2+02+1 Аr |
437 |
2249 |
1332 |
3484 |
16,80 |
|
2Н2+02+ЗАr |
382 |
1858 |
1138 |
3148 |
15,10 |
|
2Н2+02+5 Аr |
363 |
1673 |
1041 |
2832 |
13,59 |
Таблица 4.2. Результаты расчета для некоторых смесей кислород-водород-инертный разбавитель в сравнении с экспериментальными данными
|
Смеси |
Р расч, атм |
Tрасч, К- |
U0 изм, М/С |
Uо расч,/С |
|
2Н2+02 |
18,14 |
3684 |
2819 |
2866 |
|
Зн2+о2 |
17,99 |
3618 |
3197 |
3214 |
|
4Н2+02 |
17,44 |
3459 |
3425 |
3445 |
|
Н2+02 |
16,98 |
3458 |
2333 |
2331 |
|
Н2+202 |
14,47 |
2899 |
1941 |
1887 |
|
Н2+зо2 |
12,18 |
2398 |
1759 |
1641 |
|
2Н2+02+5 Аr |
13,50 |
2834 |
1700 |
1674 |
|
2Н2+02+3 Аr |
15,10 |
3148 |
1800 |
1859 |
|
2Н2+02+1,5 Аr |
16,32 |
3395 |
1950 |
2106 |
|
2Н2+02+5 Не |
13,59 |
2833 |
3160 |
3434 |
|
2Н2-O2+3 Не |
15,11 |
3148 |
3130 |
3347 |
|
2Н2+02+1,5Не |
16,32 |
3395 |
ЗОЮ |
3182 |
96
Глава 4. Развитие горения
|
|
|
|
Рис. 4.7. Зависимость скорости
Детонации от содержания
Водорода вкислородоводородной
Смеси,
* — Экспериментальные
Значения
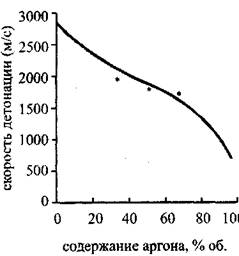
Рис. 4.8. Зависимость скорости
Детонации от содержания аргона
В стехиаметрической смеси
Водород-кислород-аргон:
* — экспериментально
Измеренные значения
|
|
|
|
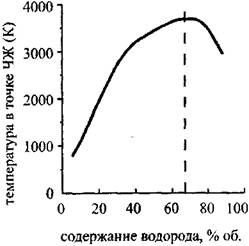
Рис. 4.9. Зависимость температуры
В точке ЧЖот содержания водорода
В кислородоводородной смеси
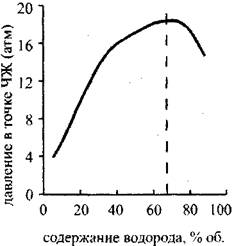
Рис. 4.10. Зависимость давления
В точке ЧЖ от содержания водорода
В кислородоводородиой смеси
97
Корольченко А. Я. Процессы горения и взрыва
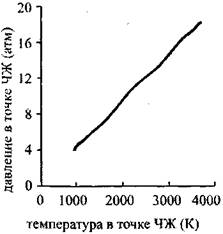
Графики зависимости температуры и давления в точке ЧЖ от содержания водорода в кислородоводородной смеси {рис. 4.9 И 4.10) Имеют максимум при 67% Н2 (гремучая смесь). Эта точка отвечает максимальному молярному энерговыделению. Зависимость температуры от давления {рис.4.11) Почти линейна, что, согласно уравнению состояния (4.21), говорит о постоянстве молярного объема в точке ЧЖ для рассмотренных концентраций водорода в смесях при одинаковых начальных условиях.
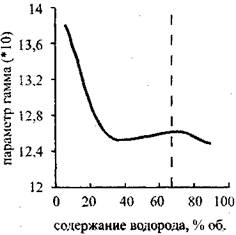
Параметр ![]() , равный отношению теплоемкостей существенно меняется при изменении состава исходной смеси. На Рис. 4.12 Изображен график зависимости
, равный отношению теплоемкостей существенно меняется при изменении состава исходной смеси. На Рис. 4.12 Изображен график зависимости ![]() От процентного содержания водорода в исходной смеси с кислородом. Резкое уменьшение значения
От процентного содержания водорода в исходной смеси с кислородом. Резкое уменьшение значения ![]() В диапазоне начальных концентраций от 6 до 38 процентов объясняется существенным увеличением в сгоревшей смеси содержания паров воды, но при дальнейшем увеличении доли водорода в исходной смеси, из-за возрастания температуры продуктов сгорания, начинает сказываться диссоциация, молекул и, в результате этого, увеличивается содержание атомарного кислорода и водорода. Это приводит к тому, что
В диапазоне начальных концентраций от 6 до 38 процентов объясняется существенным увеличением в сгоревшей смеси содержания паров воды, но при дальнейшем увеличении доли водорода в исходной смеси, из-за возрастания температуры продуктов сгорания, начинает сказываться диссоциация, молекул и, в результате этого, увеличивается содержание атомарного кислорода и водорода. Это приводит к тому, что ![]() Сгоревшей смеси перестает уменьшаться, и график, изображающий зависимость
Сгоревшей смеси перестает уменьшаться, и график, изображающий зависимость ![]() От содержания водорода в исходной смеси {рис. 4.12), Имеет небольшой максимум. Зависимость
От содержания водорода в исходной смеси {рис. 4.12), Имеет небольшой максимум. Зависимость
|
|
|
|
Рис.4.11. График,
Демонстрирующий связь между
Температурой
И давлением в точке ЧЖ
Рис. 4.12. Зависимость показателя
Адиабаты ![]() В точке
В точке
ЧЖ от содержания водорода
В киспородояодородной смеси
98
Глава 4. Развитие горения
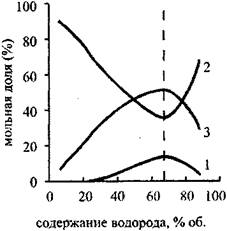
Мольных долей молекул разного вида (отличающихся числом степеней свободы) от содержания водорода в исходной смеси изображена на Рис. 4.13.
|
|
|
|
Рис. 4.13. Зависимость концентрации
Молекул разного вида от содержания
Водорода в исходной
Кислородоводородно й смеси:
1 — одноатомные молекулы;
2 — двухатомные молекулы;
3 — трехатомные молекулы
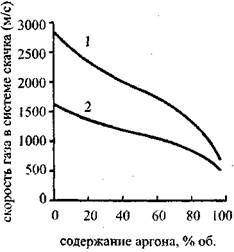
Рис. 4.14. Зависимость скорости газа
В системе отсчета, связанной с волной
От содержания аргона
В стехиометрической смеси
Водород-кислород-аргон:
1 — скорость газа на фронте;
2 — скорость газа в точке ЧЖ
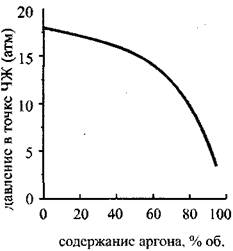
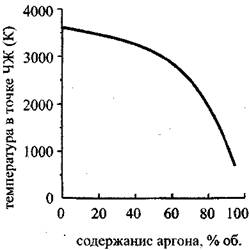
На Рис. 4.14 Представлены графики, изображающие зависимость скорости детонации и скорости звука в точке ЧЖ для смеси, состоящей из двух молей водорода, одного моля кислорода и инертного разбавителя (аргона). Видно, что вначале как скорость детонации, так и скорость звука в точке ЧЖ быстро убывают, затем зависимость становится более плавной, а затем, в области концентрации Н270-95 % опять резко убывает. Если в области концентраций аргона до 70 % уменьшение скоростей детонации и звука в точке ЧЖ объясняется уменьшением удельного энерговыделения за счет замещения части горючего и окислителя инертным аргоном, то после прохождения этой отметки резкое падение скоростей детонации и звука, а также температуры (рис. 4.15) И давления (рис. 4.16) В точке Чепмена-Жуге происходит за счет неполного сгорания.
Корольченко А. Я. Процессы горения и взрыва
|
|
|
|
Рис. 4.15. Зависимость температуры
В точкеЧЖ от содержания аргона
В стехштетрической смеси
Водород-кислород-аргон
Рис. 4.16. зависимость давления
В точке ЧЖ от содержания аргона
В стехшметрической смеси
Водород—кислород—аргон
|
|
|
|
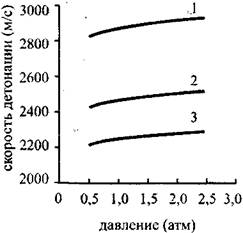
Рис. 4.17. Зависимость скорости
Детонации стехиолтпрической
Смеси водород-киашрод-аргон
От начального давления:
1-0% аргона; 2-14% аргона;
3 -25 % аргона
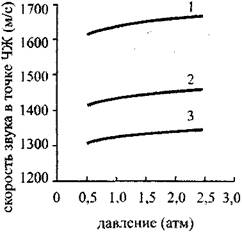
Рис. 4.18. Зависимость скорости в
Точке ЧЖ стехштетрической
Смеси водород-кислород-аргон
От начального давления:
1-0% аргона;2-14% аргона;
3-25 % аргона
100
Глава 4. Развитие горения
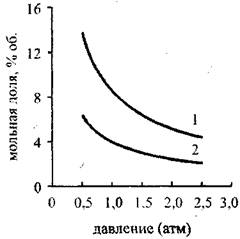
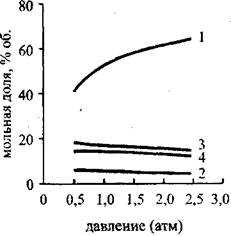
На Рис. 4.17-4.20 Представлены графики, показывающие зависимость основных химических и термодинамических параметров детонационной волны в газовой смеси, состоящей из одного моля кислорода и двух молей водорода с добавкой аргона, от начального давления в диапазоне 0,05-0,25 МПа. По графикам (рис. 4.17-4.18) Видно, что с ростом давления, скорость детонации и скорость звука в точке ЧЖ растут, причем скорость детонации растет примерно в два раза быстрее, чем скорость звука. Как следует из уравнения (4.23.), увеличение разности скорости детонации и скорости газа в точке Чепмена-Жуге говорит об увеличении удельного энерговыделения в детонирующей смеси. Это подтверждают Рис. 4.19 И 4.20, На которых изображены зависимости мольных долей различных соединений в прореагировавшей газовой смеси. По графикам видно, что с ростом начального давления подавляется диссоциация молекул, а выгорание горючего растет. Производная от скоростей по давлению практически не меняется для смесей с разным содержанием аргона, однако и скорость детонации и скорость в точке ЧЖ убывают при возрастании содержания аргона. Давление в точке ЧЖ, с ростом начального давления растет линейно, с коэффициентом роста, уменьшающимся при увеличении содержания аргона.
|
|
|
|
|
Рис. 4.20. Зависимость концентрации Молекул разного вида от начального Давления в исходной стехиометри- Ческой киаюродоводородной Смеси: 1 — Н; 2- О |
Рис. 4.19. Зависимость концентрации
Молекул разного вида от начального
Давления в исходной стехиаметри-
Ческой киаюродоводородной смеси: 1 — Н20; 2 — О2; 3 — Н2; 4-OH
101
Корольченко А. Я. Процессы горения и взрыва______________________



 7 мая, 2013
7 мая, 2013  admin
admin 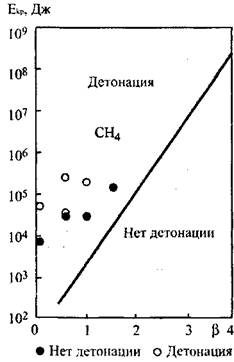
 Опубликовано в рубрике
Опубликовано в рубрике