Теоретическая температура горения /теор отличается от жаропроизводительности /max тем, что при подсчете /Теор учитывается теплота диссоциации продуктов горения. При высокой температуре СОг диссоциирует с образованием СО и Ог, а НгО — с образованием Нг и Ог.
Степень диссоциации возрастает с повышением температуры и снижением парциального давления СОг и НгО. Так, при парциальном давлении СОг, равном 0,2 кгс/см2, при сжигании углерода при атмосферном давлении в стехиометрическом объеме воздуха и содержании в продуктах сгорания 20% С02 при 1800 °С диссоциирует около 3,7% С02, при 1900°С— около 6%, при 2000°С —около 10%, при 2100°С — около 15%, при 2200°С — около 23%.
Таким образоїм, с повышением температуры диссоциация СОг быстро возрастает, и при 3000 °С диссоциирует около 90% СОг.
При понижении парциального давления СОг степень диссоциации возрастает. Так, например, при 2000°С и давлении С02, равном 1 кгс/см2, диссоциирует 6% С02 и при давлении 0,1 кгс/см2—около 12,5%.
Водяной пар диссоциирует при равных температурах и давлениях в значительно меньшей степени, чем двуокись углерода. Так, при 2000 °С и парциальном давлении 1 кгс/см2 диссоциирует около 2%, при давлении 0,2 кгс/см2 — около 3,5% и при давлении 0,1 кгс/см2—около 4% Н20.
Таким образом, степень диссоциации водяного пара при температуре 2000 °С примерно втрое меньше степени диссоциации двуокиси углерода.
При подсчете температуры в топках при сжигании топлива с высокой жаропроизводительностыо и в особенности при подогреве воздуха необходимо считаться с понижением температуры вследствие диссоциации продуктов сгорания.
Методика подсчета температуры горения с учетом диссоциации продуктов сгорания была разработана акад. Н. С. Курнаковым [50] и получила широкое применение в расчетах металлургических процессов и процессов горения. Метод подсчета в большой степени осложняется необходимостью учета изменения вследствие диссоциации двух величин — температуры и объема продуктов горения.
Следует отметить, что при высокой температуре необходимо считаться не только с диссоциацией двуокиси углерода с образованием окиси углерода и кислорода и диссоциацией водяного пара с образованием водорода и кислорода, но и с более далеко идущей диссоциацией продуктов сгорания с образованием гидроксилов и атомарного водорода и кислорода, а также с появлением в составе продуктов сгорания окиси азота NO в результате эндотермического процесса окисления азота. Так, подсчеты состава продуктов сгорания при атмосферном давлении октана (CgHie) в стехиометрическом объеме воздуха, произведенные Я. Б. Зельдовичем и А. И. Полярным, показали, что при 2127°С в составе продуктов горения содержится, %: 72,1 N2; 12,61 Н20; 9,88 С02; 2,31 СО; 1,14 ОН; 0,41 NO; 0,92 02; 0,12 Н и 0,09 О [51].
Таким образом, трудоемкий подсчет теоретической температуры горения, производимый по указанной выше методике [50], не вполне точен, поскольку учитывается только диссоциация СОг и НгО с образованием СО, Н2 и Ог и не принимается во внимание содержание в продуктах горения гидроксилов и атомарных газов. Допускаемая при этом погрешность может быть оценена следующим образом. Теплота диссоциации в пересчете на 1 м3 исходных продуктов сгорания октана равна 101 ккал с учетом образования СО, Н2 и 02 и около 108 ккал с учетом образования также закиси азота, гидроксилов и атомарных газов.
4 М. Б. Равич 97
|
Степень диссоциации двуокиси углерода
|
Следовательно, расхождение составляет около 7 ккал на 1 м3 продуктов сгорания, или около 450 ккал на 1 м3 октана.
Указанная величина составляет около 0,8% по отношению к теплоте сгорания октана. Температура горения, подсчитанная без учета более глубокой диссоциации продуктов сгорания при указанной температуре, также примерно на 0,8%, или на 15 град отличается от температуры горения, подсчитанной с более полным учетом продуктов диссоциации.
Теоретическая и расчетная температуры горения в большой степени зависят от точности заданного соотношения топлива и воздуха. Так, при увеличении избытка подаваемого воздуха на 1% расчетная температура горения снижается примерно на 0,5%. Между тем контроль процесса горения, осуществляемый по газовому анализу, в большинстве случаев не позволяет поддерживать избыток воздуха с точностью, превышающей 1%, что соответствует изменению содержания кислорода около 0,2%.
В связи с этим следует считаться с определенными погрешностями в подсчете теоретической и расчетной температур горения, производимом по принятой в настоящее время сложной и трудоемкой методике.
Как уже отмечалось, в технических расчетах при сжигании топлива без применения обогащенного кислородом воздуха и при поддержании температуры ниже 2100 °С обычно считаются с образованием в продуктах сгорания в результате диссоциации только СО, Н2 и 02. В этих случаях с учетом указанных выше погрешностей можно приближенно подсчитать теоретическую и расчетную температуры горения по простой методике, основанной на следующих положениях.
Объем продуктов сгорания в результате диссоциации С02 и Н20 возрастает, однако теплосодержание продуктов сгорания, не диссоциированных и частично диссоциированных, при той же температуре практически почти не меняется вследствие того, что объемная теплоемкость исходных трехатомных газов С02 и Н20 более высока по сравнению с теплоємкостями образующихся двухатомных газов. Так, объемная теп-
|
Давление, кгс’см2 |
||||||||||||
|
0,20 |
0,25 |
0,30 |
0,35 |
0.40 |
0,45 |
0,50 |
0,60 |
0,70 |
0.80 |
0,90 |
1,00 |
|
|
0,4 |
0,4 |
0,4 |
0,4 |
0,4 |
0,4 |
0,4 |
0,4 |
0,4 |
0,4 |
0,41 |
0,4 |
|
|
1.3 |
1,2 |
1,1 |
1,0 |
0,95 |
0,9 |
0,85 |
0,83 |
0,79 |
0,75 |
0,72 |
0,7 |
|
|
2,2 |
2,0 |
1,9 |
1,8 |
1,75 |
1,7 |
1,65 |
1.6 |
1,5 |
1.4 |
1,3 |
1.3 |
|
|
‘ 3,7 |
3,5 |
3,3 |
3,1 |
3,0 |
2,9 |
2,75 |
2,6 |
2,5 |
2.4 |
2.3 |
2,2 |
|
|
6,1 |
5,6 |
5,3 |
5,1 |
4,9 |
4,7 |
4,5 |
4.3 |
4,1 |
3.9 |
3,7 |
3,6 |
|
|
10,0 |
9,4 |
8,8 |
8,4 |
8,0 |
7,7 |
7,4 |
7.1 |
6,8 |
6,5 |
6,2 |
6.0 |
|
|
14,9 |
13,9 |
13,1 |
12,5 |
12,0 |
11,5 |
11,2 |
10,5 |
10,1 |
9,7 |
9,3 |
9,0 |
|
|
22,6 |
21,2 |
20,1 |
19,2 |
18,5 |
17,9 |
17,3 |
16,4 |
15,6 |
15,0 |
14,5 |
14,0 |
|
|
30,0 |
28,2 |
26,9 |
25,7 |
24,8 |
24,0 |
23,2 |
22,1 |
21,1 |
20,3 |
19,6 |
19,0 |
|
|
39,6 |
37,5 |
35,8 |
34,5 |
33,3 |
32,3 |
31,4 |
29,9 |
28,7 |
27,7 |
26,8 |
26,0 |
|
|
49,7 |
47,3 |
45,4 |
43,9 |
42,6 |
41,4 |
40,4 |
38,7 |
37,2 |
36,0 |
34,9 |
34,0 |
|
|
59,7 |
57,4 |
55,5 |
53,8 |
52,4 |
51,2 |
50,1 |
48,2 |
46,6 |
45,3 |
44,1 |
43,0- |
|
|
69,4 |
67,3 |
65,5 |
63,9 |
62,6 |
61,3 |
60,3 |
58,4 |
56,8 |
55,4 |
54,1 |
53,0 |
|
|
77,9 |
76,1 |
74,5 |
73,2 |
71,9 |
70,8 |
69,9 |
63,1 |
66,6 |
65,3 |
64,1 |
63,0 |
|
|
84,5 |
83,0 |
81,8 |
80,7 |
79,7 |
78,8 |
78,0 |
76,& |
75,2 |
74,0 |
73,0 |
72,0 |
|
|
89,6 |
88,5 |
87,6 |
86,8 |
86,0 |
85,4 |
84,7 |
83,6 |
82,5 |
81,7 |
80,8 |
80,0 |
Лоемкость СОг от 0 до 2000 °С равна 0,6785 ккал/’м8, теплоемкость СО 0,3592 ккал/м3 и теплоемкость кислорода 0,3748 ккал/м3 (см. табл. 36). Следовательно, теплосодержание 1 м3 СО и 0,5 м3 Ог, образующихся в результате диссоциации 1 м3 СОг, мало отличается от теплосодержания исходной С02:
Ссо + 0,5С0б=0,3592 + 0,5-0,3748==0,5466 ккал/(мэС02• °С).
По отношению к теплосодержанию исходной СОг разность составляет
Гг. ____ (0,5466 — 0,5785)-100 к0/
————— 075785————— ~&/0-
Теплосодержание продуктов диссоциации 1 м3 НгО в большей степени отличается от теплосодержания исходного водяного пара:
Сн^о000=0,4688 ккал/(м8.°С);
Сн^2000 + 0,5-СЙ72000=0,3362 + 0,5-0,3748=0,5236 ккал/(м3Н20-°С);
Нп (0,5236 — 0,4688).100 . ,, 0/
TlaU=—————- 0~4688———- = +И /о-
Итак, теплосодержание продуктов диссоциации СОг несколько ниже теплосодержания исходной двуокиси углерода, а теплосодержание продуктов диссоциации НгО выше, чем у исходного водяного пара.
С учетом того, что СОг диссоциирует в сопоставимых условиях в -большей степени, чем водяной пар, суммарные отклонения в теплосодержании продуктов диссоциации и исходных газов у большинства видов топлива в значительйой степени нивелируются.
Поскольку при температурах до 2100 °С диссоциирует лишь малая часть СОг и Н20 и, следовательно, еще меньшая часть суммарного •объема продуктов сгорания топлива, содержащих высокий процент азо-
4* 99
|
Степень диссоциации водяного пара
|
Та, можно для упрощенного подсчета теоретической и расчетной температур горения принять, что произведение объемов продуктов сгорания на их средневзвешенную теплоемкость в температурном интервале от О до £теор не меняется в результате диссоциации СОг и Н20 [37].
При таком допущении теоретическую температуру горения можно подсчитать по формуле
Где Qя — низшая теплота сгорания топлива, ккал/кг или ккал/м3; <3дис — теплота диссоциации продуктов сгорания, образующихся при сгорании 1 кг или 1 м3 топлива, ккал/кг или ккал/м3; V—объем продуктов сгорания, м3/кг или м3/м3; С—средневзвешенная теплоемкость продуктов сгорания от 0 до £Теор ккал/м3-°С.
Значения средневзвешенной теплоемкости продуктов сгорания от 0 до t приведены в табл. 36.
Следовательно, упрощенный подсчет теоретической температуры горения £теоР отличается от подсчета жаропроизводительности £тах лишь необходимостью учета теплоты диссоциации <ЗДИс.
Данные о степени диссоциации СОг и НгО при различных температурах и парциальных давлениях приведены в табл. 45 и 46.
Приведем пример подсчета теоретической температуры горения пропана.
Низшая теплота сгорания пропана 21 800 ккал/м3. Уравнение горения пропана в стехиометрическом объеме воздуха
С8Н„ + 502 + 5-3,76N2 = ЗС02 + 4Н20 + 18,8N2.
Объем продуктов сгорания 25,8 м3.
Состав продуктов сгорания, %: 11,5 С02; 15,’5 Н20; 73,0 N2.
Задаемся температурой горения 2000 °С и подсчитываем значение теплоты диссоциации С02 и Н20 при парциальных давлениях 0,115 и 0,155 кгс/см2 и температуре 2000 °С. Степень диссоциации С02 а=0,12 (таїбл. 45).
|
Давление, кгс/см2
|
Теплота диссоциации СОг:
<2дисУсо2• aQco = 3• 0,12■ 3030 = 1090 ккал.
Степень диссоциации НгО 6=0,036 (табл. 46).
Теплота диссоциации НгО:
= УЩО бН2 = 4-0,36-2580 = 370 ккал.
Суммарная теплота диссоциации
<5дис = Се2 + = ‘090 + 370 = 1460 ккал.
Теоретическая температура горения
QH — Ол„о 21 800 — 1460
‘теор = Чн усМС = 25.8.о,4 = 1970°С = 2240
На рис. 10 приведены для сопоставления значения теоретической температуры горения при атмосферном давлении некоторых углеводородов. Теоретическая температура горения пропана при а=1 равна около 2250 °К.
Подсчитанная аналогичным образом по упрощенной методике теоретическая температура горения метана равна 1930 °С, или 2200°К.
Значение теоретической температуры горения метана по этому графику равно 2220°К. Теоретическая температура горения бензола, подсчитанная по формуле (VII.20), равна 2060 °С, или около 2330 °К и мало отличается от температуры, приведенной на указанном графике (2340°К).
Таким образом, для определения теоретической температуры горения, развиваемой в условиях сжигания топлива в воздухе (до 2100°С), можно пользоваться достаточной для технических расчетов степенью точности простой методикой подсчета [37].
При *тах порядка 2200°С ^е0р== ‘max-0,93, а при /max порядка 2100°С
‘теор =’max — 0,94.
При сжигании топлива в кислороде или обогащенном кислородом воздухе при значительно более высоких температурах необходимо под^
101
|
|
|
І. юо |
|
Рис. 10. Теоретические и расчетные температуры горения углеводородов |
|
1,0 !,1 1,2 1,3 |
Считывать температуру горения с учетом образования сложной гаммы продуктов диссоциации. В этих случаях различие между теоретической температурой горения и жаропроизводительностью, подсчитываемой без учета диссоциации, очень велико (рис. 11).
Теоретическую температуру горения, подсчитанную при сжигании в абсолютно сухом воздухе, обозначают £геор, а при учете содержания в воздухе 1% (по массе) Н20 .
|
Woo |
Различие между и /Теор — около 30°С, ^еор =/теор — 30°С.
|
/ |
|
, 3500 % І Ti 2000 Її Iі IS00 К £ |
|
2000 |
|
7000 |
|
3000 Ш0 5000 ЖаропраиздоНителЬностб, °С |
|
Рис. 11. Соотношения жаропроизводительности и теоретической температуры горения топлива |



 2 сентября, 2012
2 сентября, 2012  admin
admin 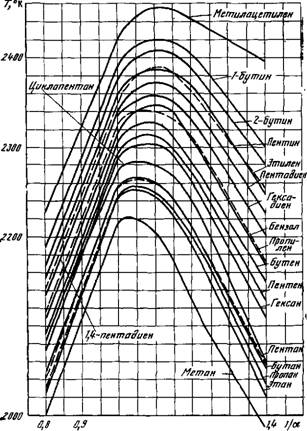
 Опубликовано в рубрике
Опубликовано в рубрике